Propriedades Químicas e Físicas da Matéria:
As características específicas de cada material constituem as propriedades organolépticas da matéria.
Por exemplo: O queijo = Cada um terá cor específica, odor específico e sabor específico.
As características observadas em qualquer objeto, independente do material que é feito, faz parte das propriedades gerais da matéria.
Propriedades Gerais:
- Extensão: Toda matéria ocupa um lugar no espaço.
- Inércia: Os corpos se mantem em repouso ou em movimento até que uma força atue neles.
- Impermeabilidade: Dois corpos não ocupam o mesmo lugar no espaço.
- Compressibilidade: A matéria diminui seu volume sob a ação de uma força.
- Elasticidade: A matéria retorna ao volume original, após ser comprimida.
- Divisibilidade: Toda matéria pode ser dividida em partes menores.
- Descontinuidade: Toda matéria é descontínua, ainda que pareça compacta demais. Existem espaços entre uma molécula e outra, sendo, que quanto maior esses espaços, mais mole ela será e, consequentemente, quanto menor esses espaços, mais rígida ela será.
Propriedades Específicas:
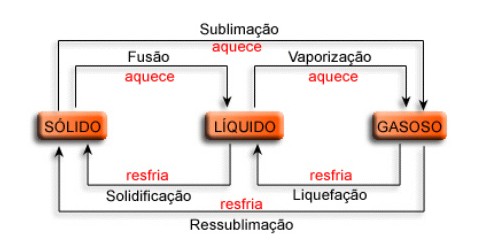
- Temperatura de Fusão: Temperatura onde um material passa do estado sólido para o líquido.
- Temperatura de Solidificação: Temperatura onde o material passa do estado líquido para o sólido.
- Temperatura de Ebulição: Temperatura onde o material passa do estado líquido para o gasoso.
- Condutividade: Capacidade de conduzir eletricidade.
- Magnetismo: Capacidade de atrair imã.
- Dureza: Resistência ao risco.
- Maleabilidade: Capacidade de ser moldado.
- Ductibilidade: Capacidade de ser transformado em fio.
- Densidade: Relação entre a massa e o volume do material.
*As propriedades específicas mais utilizadas no dia a dia são as Temperaturas de Fusão e Ebulição e Densidade.
A Densidade da matéria depende da temperatura, já que o volume da matéria pode variar quando aquecido ou resfriado. Logo, a temperatura deve ser relacionada quando for levar em conta a densidade!
Geralmente, a densidade é medida em temperatura ambiente (25°C). A unidade da densidade é expressa em g/cm³, de acordo com o Sistema Internacional (SI).
Resumindo: A densidade relaciona massa e volume.
Sua fórmula é: d = m/v ou d = m
v
Já que a densidade depende da temperatura, devido à variação do volume quando aquecido ou resfriado, pode-se afirmar que a densidade de um material será diferente em cada estado físico. (Sólido, Liquido e Gasoso)
Atenção: A densidade de um mesmo material no estado gasoso é menor que a sua densidade no estado líquido e sólido.
Por que?
Pois a proximidade entre as partículas do material é menor no estado gasoso, variando mais o estado físico, ou seja, forma volume diferente, mais disperso e menos denso.
(Se a proximidade entre as partículas é menor, significa que estão mais longe uma da outra, tendo mais espaço para se movimentarem, o que torna o material menos denso, mais maleável e com maior volume)
No entanto, a Água apresenta tem uma característica diferente dos outros materiais. Ao se solidificar, o seu volume se expande.
Por que?
Devido às forças de interação entre suas moléculas e ao arranjo espacial da água no estado sólido.
*Por isso o gelo flutua sob a água.
Gostou? Em breve tem mais! Veja os exercícios sobre essa matéria e muitas outras.